‘KLS-2031’은 기존 신경병증성 통증 치료 방식과는 달리, 특허 받은 유전자 조합을 이용한 주사 요법의 치료제다. 1회 국소 주사 시술방식으로 진통 효능이 장기간 지속되고 근원적 치료가 가능하도록 개발됐으며, 기존 시판된 치료제로는 효과를 보지 못하는 신경병증성 통증 환자가 타겟이다.
‘신경병증성 통증’은 신경계의 손상이나 기능적 이상으로 발생하는 난치성 통증으로, 환자들에게 극심한 고통을 주는 감각신경계 질환이다. 해당 병증의 주된 치료제는 진통제 계열로 지속적 효과 및 근원적 치료가 불가능하다. 또한 최종 진통제로 주로 쓰이는 아편(Opioid)계열의 약은 마약성을 가지고 있어 미국 내 미충족 의료(Unmet medical need)가 매우 높은 질환이다.
코오롱생명과학은 작년 3월 미국 식품의약안전처(FDA)로부터 KLS-2031의 임상시험계획(IND)을 승인받았으며, 12월 미국 내 임상기관과의 연구윤리심의위원회(IRB)의 첫 승인을 마쳤다. 오는 3월부터 첫환자 방문을 시작으로 미국내 2개의 임상 기관을 통해 KLS-2031의 안전성 및 유효성 평가를 목적으로 임상 1상/2a상이 진행될 예정이다.
KLS-2031 임상 1상/2a상의 대상자는 총 18명으로 투약 후 24개월간 추적 관찰한다. 이를 통해 이후 임상 단계 진행 방향을 결정한다. KLS-2031은 신경병증성 질환 중 요천골 신경근병증 통증에 대한 혁신 신약(First in class) 후보물질로, 이번 패스트 트랙 지정으로 기간 단축등의 혜택을 받아 일정은 더욱 앞당겨질 예정이다.
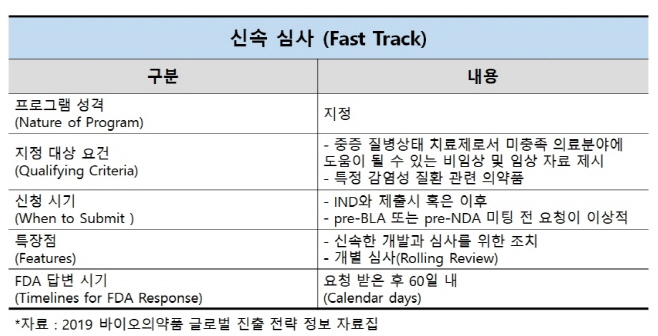
이번에 지정된 ‘패스트 트랙’은 신약을 짧은 기간내에 개발할 수 있도록 만든 미국 FDA의 제도로, 미국에서 의약품을 출시하는 가장 빠른 방법중의 하나다. 심각한 질환(Serious Disease)이나 미충족 의료(Unmet medical need)가 높은 질환에 대한 약물의 개발을 신속히 진행하기 위해 도입된 제도이다.
KLS-2031은 개발기간 중 FDA와 신속한 사전협의, 각 임상단계별 동반 심사(Rolling review)등을 통해 심사기간을 단축하고 최종 승인 확률을 높이게 된다. 임상 3상 이후 신청가능한 우선 심사(Priority review)를 통해 심사기간을 더욱 단축할 수 있다.
코오롱생명과학 관계자는 “향후 KLS-2031은 요천골 신경근병증 뿐만 아니라 다른 신경병증성 통증질환에도 확장성을 가질수 있는 신약으로 개발 될 것”이라며 “앞으로 커져가는 통증 치료 분야에서 근원적 치료제로 만들기 위해 글로벌 파트너사와의 밀접한 커뮤니케이션을 통해 해외 진출의 다양한 방향을 모색할 계획”이라고 말했다.
한편 전세계적으로 통증관련 시장은 2016년 23조원 규모에서 2023년 34조원 가량의 규모로 연평균 5프로 이상 성장할 것으로 예측된다. 이 중 KLS-2031가 관련된 신경병증성 통증 시장은 2022년 4조원에 달하는 규모가 될 것으로 예상한다.
|