FDA에 1상 임상시험계획 제출
"전사 역량 집중해 임상시험 속도"
|
한미약품은 지난달 말 미국 식품의약국(FDA)에 '신개념 비만치료제(HM17321)'의 임상1상 진입을 위한 임상시험계획(IND)을 신청했다고 1일 밝혔다.
HM17321은 단순히 근손실을 보완하는 수준을 넘어, 기존에 불가능하다고 여겨졌던 '근육량 증가'와 '지방 선택적 감량'을 동시에 구현하는 세계 최초의 비만 혁신 신약(First-in-Class)으로 개발되고 있다. 이번 임상시험은 건강한 성인을 대상으로 HM17321의 안전성과 내약성, 약동학, 약력학 특성 등을 평가할 계획이다.
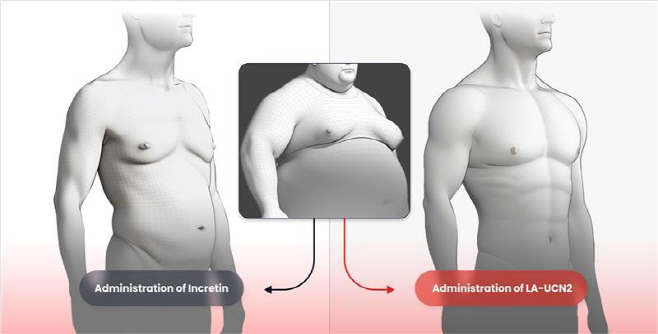
HM17321은 GLP-1을 비롯한 인크레틴 수용체가 아닌 CRF2(corticotropin-releasing factor 수용체를 선택적으로 타깃하는 UCN2(Urocortin-2) 유사체다. 한미약품 R&D센터에 내재화된 최첨단 인공지능 및 구조 모델링 기술을 활용해 설계됐다. CRF는 스트레스 반응과 관련된 신호 분자로, 그 수용체 중 CRF2 수용체를 선택적으로 타깃하면 지방 감소와 근육 증가, 근기능 개선 등을 직접 이끌어낼 수 있다는 게 한미약품 설명이다.
한미약품은 최근 유럽당뇨병학회(EASD 2025)에서 발표한 '비만 영장류(Rhesus monkey) 모델' 연구를 통해 HM17321이 체지방은 감량하면서 동시에 제지방량을 보존하는 효과를 재차 확인했다. HM17321은 단독요법 뿐만 아니라, 기존 인크레틴 계열 비만 치료제와의 병용요법에서도 양적·질적으로 우수한 체중감량 효과를 나타냈다.
대부분의 항체 기반 근육 보존 약물들은 정맥 투여 방식으로 인해 비만 환자들에게 사용 편의성이 떨어진다. 또한, 피하 투여 방식의 기존 비만 치료제와의 병용 시 투여 방법 차이로 인한 한계가 지적된다. 한미약품 측은 "HM17321은 병용 치료제로 개발될 경우, 동일한 펩타이드 형태인 기존 인크레틴 계열 약물과 한 번에 투약할 수 있어 환자 편의성이 크게 향상할 것으로 기대된다"고 설명했다.
한미약품은 HM17321의 상용화 목표 시점을 2031년으로 설정하고, 전사적 역량을 집중해 임상 개발을 속도감 있게 추진해 나간다는 계획이다.
최인영 R&D센터장(전무)은 "한미의 신약개발 전략은 비만 치료를 단순한 체중 감량 경쟁으로 보지 않고, 환자들이 장기적으로 건강한 삶을 설계하고 유지할 수 있는 여정으로 바라보는 데 핵심을 두고 있다"며 "HM17321은 '지방 감량과 근육 증가, 운동 및 대사 기능 개선'이라는 통합적 효능을 동시에 지향하기에 근감소증 및 고령층 비만, 운동 기능 저하 환자군 등 미충족 수요를 해결하며 곧 다가올 미래에 혁신적 치료제로 자리매김할 것으로 확신한다"고 말했다.